Hypoxie: meer dan alleen zuurstoftekort
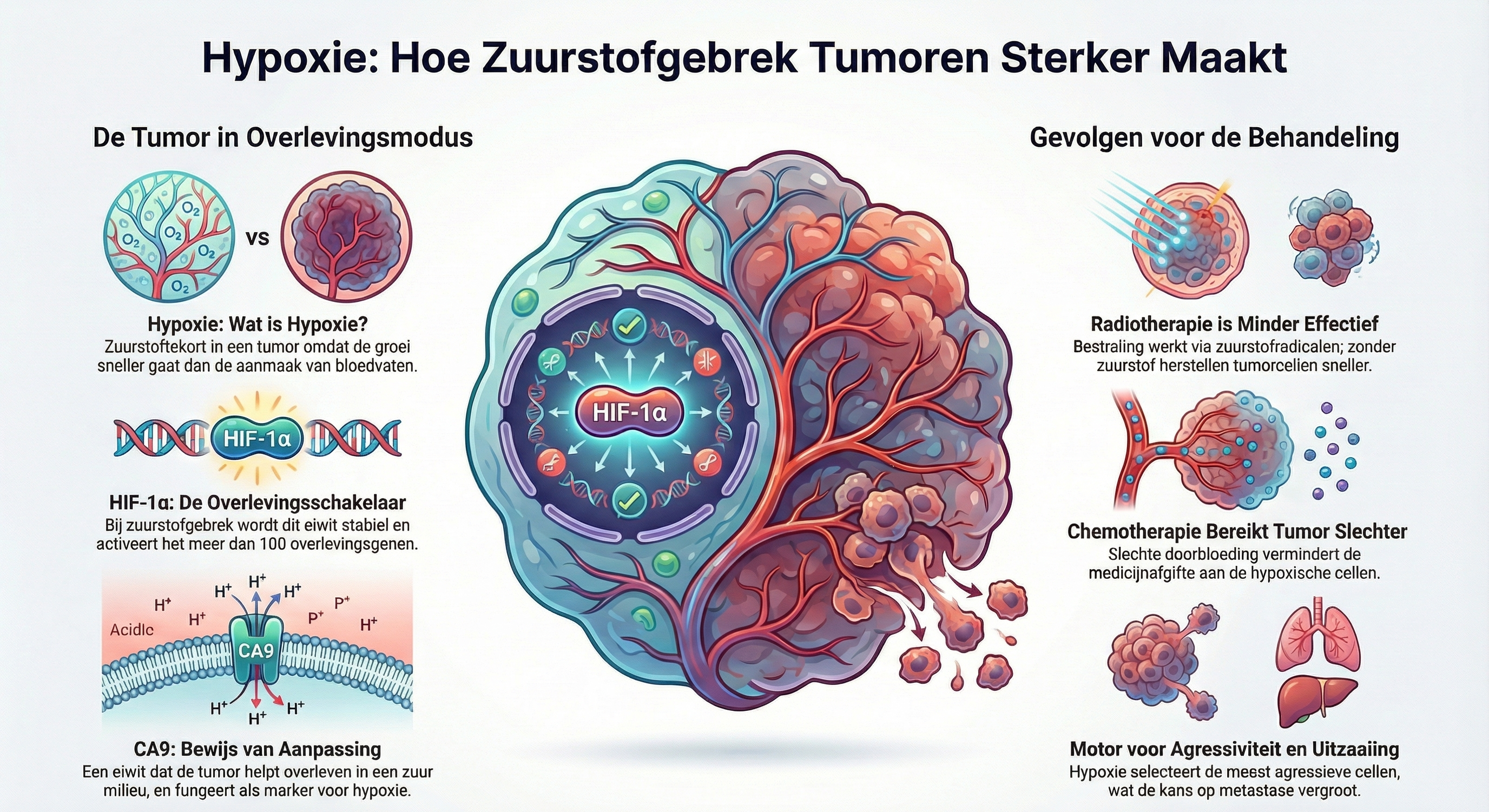
Veel solide tumoren groeien sneller dan hun bloedvoorziening kan aanleggen. Hierdoor ontstaan gebieden met zuurstoftekort, ook wel hypoxie genoemd. Dit is geen passief bijproduct van tumorgroei; het verandert de tumor biologisch op wezenlijke wijze. Hypoxische tumoren worden agressiever, muteren sneller en reageren slechter op therapie. Het is dan ook geen toeval dat hypoxie al jaren wordt herkend als een belangrijke negatieve prognostische factor.
HIF-1α: de overlevingsschakelaar onder stress
Het lichaam heeft een ingenieus systeem om met zuurstoftekort om te gaan. De centrale regulator hierin is de Hypoxia-Inducible Factor (HIF), bestaande uit een zuurstofgevoelige α-subeenheid en een altijd aanwezige β-subeenheid.
In normale zuurstofcondities wordt HIF-α snel afgebroken. Het enzym PHD markeert het eiwit zodat het via het VHL-eiwit kan worden vernietigd in de proteasoom. Maar zodra de zuurstofspanning daalt, stopt deze afbraak. HIF-α blijft stabiel, verplaatst zich naar de celkern en begint meer dan honderd genen te activeren die cellen helpen overleven.
Daarmee verandert de tumor in een biologische overlevingsmachine. Hij stimuleert bloedvatvorming via VEGF, versterkt groeisignalen via PDGF en past zijn metabole huishouding aan met behulp van CAIX. Hypoxie is dus geen zwakte; het is een evolutionair voordeel voor de tumor.
CA9: bewijs dat een tumor zich heeft aangepast
Eén van de opvallendste doelwitten die door HIF worden geactiveerd, is Carbonic Anhydrase 9 (CA9). Tumorcellen produceren onder hypoxische omstandigheden veel lactaat en zuren. Zonder compensatie zou dit fataal zijn. CA9 helpt de pH te reguleren, voert protonen af en zorgt dat de cel in leven kan blijven in een zuur milieu.
Omdat CA9 vrijwel uitsluitend hoog wordt uitgedrukt in hypoxische tumoren, wordt het gebruikt als marker voor hypoxie, als tumormarker en zelfs als hulpmiddel bij prognose-inschatting. In tumoren zoals clear cell niercelcarcinoom, waar VHL vaak gemuteerd is, blijft HIF-α continu actief en zie je daardoor sterke CA9-expressie, onafhankelijk van de zuurstofconditie.
Waarom hypoxische tumoren moeilijker te behandelen zijn
Hypoxie heeft directe klinische consequenties. Radiotherapie werkt grotendeels via zuurstofradicalen. Wanneer er weinig zuurstof beschikbaar is, worden DNA-schades minder stabiel en herstellen tumorcellen sneller, waardoor bestraling minder effectief is. Hypoxische tumoren zijn daardoor tot enkele keren radioresistenter.
Ook chemotherapie heeft het moeilijker. Slechte doorbloeding betekent slechtere medicijntoediening. Daarnaast activeren hypoxische cellen overlevingsmechanismen en muteren ze sneller, waardoor resistentie ontstaat. Niet zelden blijken terugkerende tumoren nóg hypoxischer en daardoor nóg lastiger te behandelen.
Toch biedt hypoxie ook behandelstrategische mogelijkheden. Tijdens bestralingsschema’s kan zogenaamde reoxygenatie optreden: tumorcellen die eerder slecht bereikbaar waren, krijgen opnieuw toegang tot zuurstof wanneer andere cellen afsterven. Hierdoor worden latere bestraling sessies effectiever.
Hypoxie als motor voor agressiviteit
Hypoxie creëert een vorm van natuurlijke selectie binnen de tumor. Cellen die zich kunnen aanpassen, overleven; cellen die dat niet kunnen, sterven. Wat overblijft, is een populatie cellen die agressiever, mutatiegevoeliger en mobieler is. Het is dan ook niet verwonderlijk dat hypoxie wordt geassocieerd met een grotere kans op metastasen en slechtere klinische uitkomsten.
Conclusie
Hypoxie is veel meer dan zuurstofgebrek. Het is een motor achter tumoraanpassing, therapieresistentie en agressiviteit. Via HIF-1α en CA9 ontwikkelen tumorcellen slimme strategieën om te overleven in extreem vijandige omstandigheden. Het begrijpen van deze mechanismen is essentieel om toekomstige behandelingen gerichter, persoonlijker en effectiever te maken.